Ν. Ζήρας MD, PhD
Παθολόγος-Ογκολόγος
Πρόεδρος Ελληνικής Εταιρείας Νευροενδοκρινών Όγκων (EENO)
Νευροενδοκρινή Νεοπλάσματα (ΝΕΝ): Σφαιρική Ανασκόπηση
- Εισαγωγή
- Ταξινόμηση ΝΕΝ
- Κλινικά χαρακτηριστικά νευροενδοκρινών όγκων (NET, NEN G1/G2)
- Διαγνωστική προσέγγιση ΝΕΤ
- Θεραπευτική αντιμετώπιση ΝΕN: Πεδίο προκλήσεων και αναζητήσεων
- Ανάλογα σωματοστατίνης (SSA)
- Τυχαιοποιημένες μελέτες καθιέρωσης εγκεκριμένων συστηματικών θεραπειών ΝΕΝ
- Αντιμετώπιση καρκινοειδούς συνδρόμου
- Θεραπευτικοί αλγόριθμοι προχωρημένων εντεροπαγκρεατικών ΝΕΝ - Συστηματική θεραπεία πρώτης γραμμής προχωρημένων ΝΕΝ - Θεραπευτικές επιλογές NEC/NETG3
- Παρατηρήσεις και επισημάνσεις στη διαχείριση ΝΕΝ
- Εξελίξεις και προοπτικές
- Βιβλιογραφία
1. Εισαγωγή
Τα νευροενδοκρινή νεοπλάσματα (ΝΕΝ) αποτελούν ετερογενή ομάδα σπάνιων όγκων εξορμώμενων από ενδοκρινικά κύτταρα (enterochromaffin cells) που βρίσκονται διάχυτα παντού στο σώμα και μπορούν να παράγουν 50 και πλέον πολυπεπτίδια ή αμίνες (1).
Η ενασχόληση με αυτούς τους όγκους ξεπερνά την 100ετία και έχει πρωτοπόρο τον Oberndorfer που το 1907 χρησιμοποίησε για πρώτη φορά τον όρο karzinoide για να περιγράψει μια ομάδα εντερικών όγκων με συμπεριφορά λιγότερη επιθετική από τα αδενοκαρκινώματα. Στην ιστορική τους διαδρομή έχουν χρησιμοποιηθεί διάφοροι ορισμοί, όπως καρκινοειδή, νευροενδοκρινείς όγκοι (neuroendocrine tumors - NET), με επικράτηση τελικά των όρων νευροενδοκρινή νεοπλάσματα (neuroendocrine neoplasms - NEN) και νευροενδοκρινή καρκινώματα (neuroendocrine carcinomas - NEC).
Στα νευροενδοκρινή νεοπλάσματα περιλαμβάνονται (2):
- Γαστρεντερικά NEΝ
- Όγκοι κυττάρων νησιδίων παγκρέατος (Islet cell tumors)
- Φαιοχρωμοκύττωμα / Παραγαγγλίωμα
- Νευροενδοκρινή νεοπλάσματα πνεύμονα
– καρκινοειδές,
– άτυπο καρκινοειδές
– πτωχά διαφοροποιημένα καρκινώματα
– εκ μεγάλων κυττάρων
– μικροκυτταρικό
- Καρκίνωμα κυττάρων Merkel
2. Ταξινόμηση ΝΕΝ
Ταξινόμηση ΝΕΝ ανάλογα με την εμβρυϊκή τους προέλευση (3,4)
– Όγκοι πρόσθιου εντέρου (foregut tumors):
αναπτυσσόμενοι στην αναπνευστική οδό, θύμο, οισοφάγο, στομάχι, 12/λο και πάγκρεας
– Όγκοι μέσου εντέρου (midgut tumors):
αναπτυσσόμενοι στο λεπτό έντερο, σκωληκοειδή απόφυση, τυφλό και ανιόν κόλον
– Όγκοι τελικού εντέρου (hindgut tumors):
αναπτυσσόμενοι στο εγκάρσιο κόλον, κατιόν κόλον, σιγμοειδές και ορθό
Ταξινόμηση NEΝ ανάλογα με το βαθμό διαφοροποίησης, WHO 2004 (5)
– Kαλά διαφοροποιημένοι νευροενδοκρινείς όγκοι (Well-differentiated neuroendocrine tumors - NET), με νωθρή συνήθως εξέλιξη.
– Πτωχά διαφοροποιημένα νευροενδοκρινή καρκινώματα (Poorly differentiated neuroendocrine carcinomas - NEC), με επιθετική κλινική πορεία.
– Καλά διαφοροποιημένα νευροενδοκρινή καρκινώματα (Well-differentiated neuroendocrine carcinomas - NEC), με ενδιάμεση κλινική συμπεριφορά.


3. Κλινικά χαρακτηριστικά νευροενδοκρινών όγκων (NET, NEN G1/G2)
– Θεωρούνται σπάνια με τη συχνότητά τους να κυμαίνεται από 3/100.000 έως 6/100.000, αν και σε νεκροψίες είναι σημαντικά μεγαλύτερη (6,7).
– Η συχνότητά τους παγκοσμίως έχει συνεχή αυξητική τάση και στις ΗΠΑ στο διάστημα 1975-2004 έχει πενταπλασιασθεί. Τα αίτια αυτής της αύξησης είναι ασαφή μπορεί όμως να συνεισφέρουν η βελτίωση των διαγνωστικών μεθόδων, η εγρήγορσή αναζήτησής τους και ίσως περιβαλλοντικοί παράγοντες (8,9).
– Η βιολογική συμπεριφορά των ΝΕΝ είναι αβέβαιη και πολυπαραγοντική.
– Συνήθως έχουν μακρά πορεία με περιόδους εξάρσεων και σταθεροποιήσεων, γεγονός που δικαιολογεί την προσομοίωσή τους με τη ζέβρα και τις χαρακτηριστικές ασπρόμαυρες ρίγες της.
– Η διάγνωσή τους συχνά καθυστερεί και σε ποσοστό περίπου 27% είναι ήδη εξ αρχής μεταστατικά (8,10).
– Μεταστατική δυνατότητα έχουν ακόμα και μικροί όγκοι (≤5 mm) (11).
– Η πρόγνωση των ασθενών με νευροενδοκρινή νεοπλάσματα εξαρτάται από το βαθμό διαφοροποίησης του όγκου και το στάδιο της νόσου. Ασθενείς με μεταστατικά ΝΕΝ καλής/μέτριας διαφοροποίησης (G1/G2) έχουν διάμεση επιβίωση 33μηνών, παρόμοια με εκείνη άλλων καρκίνων σταδίου IV. Ασθενείς με τοπικoπεριοχική νόσο έχουν ευνοϊκότερη έκβαση. Η διάμεση επιβίωση είναι 18,5 έτη για την τοπική νόσο και 9,3 έτη για νόσο με περιοχική και μόνο επέκταση. Τη χειρότερη πρόγνωση έχουν οι μεταστατικοί πτωχά διαφοροποιημένα όγκοι (8).
– Ανάλογα με την ορμονική τους δραστηριότητα ταξινομούνται σε λειτουργικά ή μη.
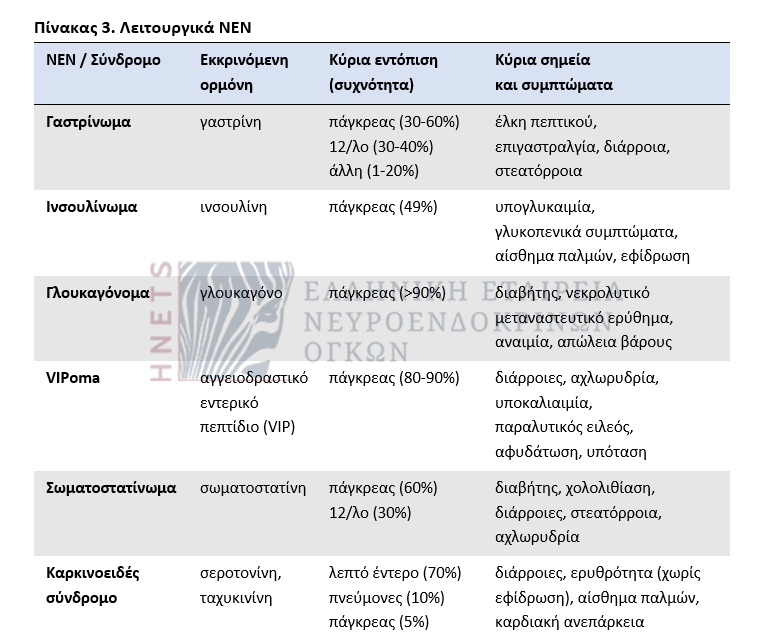
4. Διαγνωστική προσέγγιση ΝΕΤ
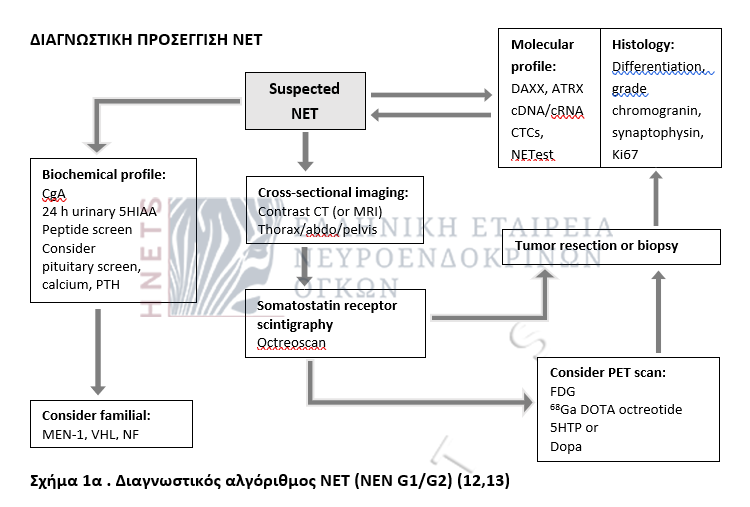
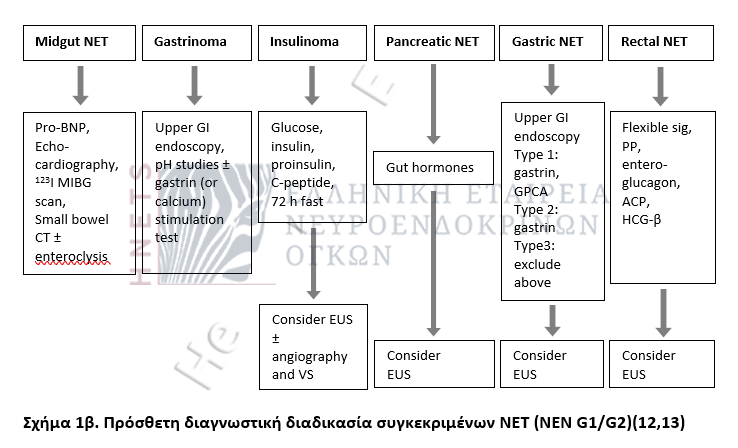
ACP: acid phosphatase, ATRX: a transcriptional regulator also known as ATP-dependent helicase ATRX, X-linked helicase II, or X-linked nuclear protein (XNP) encoded by the ATRX gene, BNP: brain natriuretic peptide, cDNA: complementary DNA synthesized from a single-stranded RNA (e.g. mRNA or miRNA) template in a reaction catalyzed by the enzyme reverse transcriptase, CgA: chromogranin A, cRNA: complementary RNA, CTC: a general stress protein encoded by the CTC gene and playing an important role in structures known as telomeres, DAXX: also known as death-associated protein 6, a protein encoded by the DAXX gene, EUS: endoscopic ultrasound, FDG: fluorodeoxyglucose, GI: gastrointestinal, GPCA: gastric parietal cell autoantibody, HCG-β: human chorionic gonadotrophin-β, 5HIAA: 5-hydroxyindoleacetic acid, 5HTP: 5-hydroxytryptophan, Men-1: multiple endocrine neoplasia 1, MIBG: meta iodobenzylguanidine, NETest: a multianalyte liquid biopsy that measures neuroendocrine tumor gene expression in blood; more specific than serum CgA, NF: neurofibromatosis, PET: positron emission tomography, PP: pancreatic polypeptide, PTH: parathyroid hormone, VHL: Von Hippel Lindau.
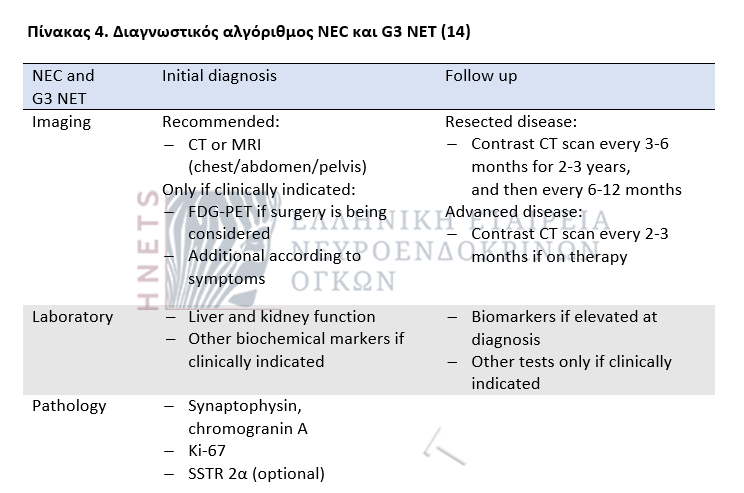
5. Θεραπευτική αντιμετώπιση ΝΕN: Πεδίο προκλήσεων και αναζητήσεων
Θεραπευτικές επιλογές
- Στην τοπική νόσο θεραπεία εκλογής είναι η ριζική χειρουργική εξαίρεση.
- Στη μεταστατική νόσο οι θεραπευτικές δυνατότητες μέχρι πρόσφατα ήταν περιορισμένες αλλά πλέον υπάρχει σημαντική πρόοδος με διεύρυνση των θεραπευτικών επιλογών και συνεχιζόμενη εντατική έρευνα. Η εξελίξεις σχετίζονται με την αναγνώριση του μοριακού υπόβαθρου των ΝΕΝ, την ανάδειξη του ρόλου σημαντικών βιόδρομων, την τεκμηρίωση της αντινεοπλασματικής δράσης των ανάλογων σωματοστατίνης και την αποτελεσματική χρήση στοχευτικών παραγόντων και ραδιοπεπτιδίων.
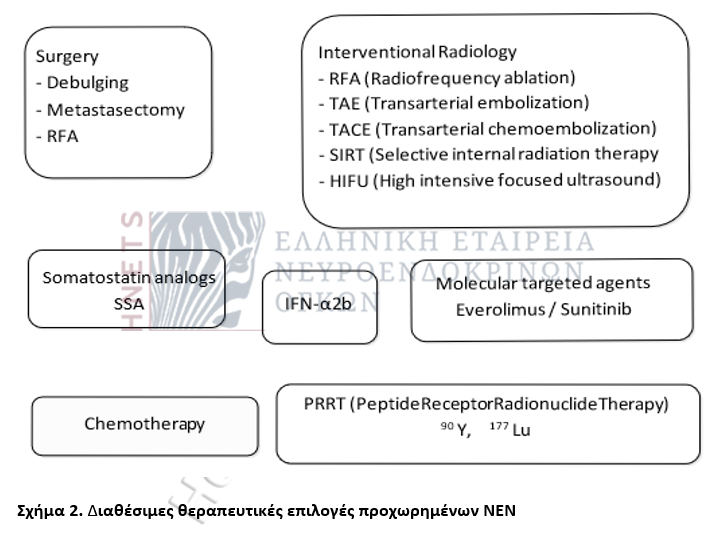
Θεραπευτικοί στόχοι
- Η χειρουργική εκτομή του πρωτοπαθούς όγκου και η εξαίρεση, εφόσον εφικτή, των μεταστατικών εστιών
- Ο έλεγχος των συμπτωμάτων
- Ο έλεγχος της προόδου της νόσου στα προχωρημένα της στάδια
- Η μέριμνα για την ποιότητα ζωής του ασθενούς
Κριτήρια καθορισμού της κάλλιστης θεραπευτικής επιλογής
- Η κλινική κατάσταση του ασθενούς και τα συνοδά του παθολογικά προβλήματα
- Η εντόπιση της πρωτοπαθούς εστίας
- Τα ιστολογικά, ανοσοϊστοχημικά και μοριακά χαρακτηριστικά του όγκου
- To φορτίο της νόσου και η βιολογική της συμπεριφορά
- H θετικότητα των υποδοχέων σωματοστατίνης στο Octreoscan ή στο Ga-68 PET-CT
- Η παρουσία καρκινοειδούς συνδρόμου, καρδιακής νόσου ή ίνωσης μεσεντερίου
- Οι προτιμήσεις ασθενούς του κατόπιν επαρκούς ενημέρωσής του
- Οι διαθεσιμότητα θεραπευτικών μεθόδων και το κόστος τους
Θεραπευτικοί προβληματισμοί και ερωτήματα
- Χρειάζονται θεραπεία όλοι τα ΝΕΝ; Ποιος ο κατάλληλος χρόνος θεραπευτικής παρέμβασης;
- Πότε επιδιώκουμε υποσταδιοποίηση και πώς;
- Προγραμματίζουμε χειρουργική εξαίρεση μεταστατικών εστιών;
- Απαιτείται επικουρική θεραπεία;
- Ποια είναι η κατάλληλη αλληλουχία των διαθέσιμων θεραπευτικών επιλογών;
- (SSTA - Στοχευτικοί παράγοντες - Χημειοθεραπεία - PRRT - RFA/TAE/TACE/SIRT)
- Έχει ρόλο η συνδυασμένη εφαρμογή PRRT και χημειοθεραπείας;
- Έχει θέση η ανοσοθεραπεία;
- Ποιο είναι το κατάλληλο πρόγραμμα παρακολούθησης ανάλογα με τον τύπο ΝΕΝ;
Αντιμετώπιση NEN: Ανάγκη διεπιστημονικής προσέγγισης
- Η σχετική σπανιότητα των ΝΕΝ, οι ιδιαιτερότητες και η πολυπλοκότητά τους απαιτούν τη διεπιστημονική συνεργασία διαφόρων ειδικοτήτων συμπεριλαμβανομένων Παθολόγων Ογκολόγων, Γαστρεντερολόγων, Χειρουργών, Παθολογοανατόμων, Ενδοκρινολόγων, Πνευμονολόγων, Πυρηνικών Ιατρών και Παρεμβατικών Ακτινολόγων.
6. Ανάλογα σωματοστατίνης (SSA)
Τα ανάλογα σωματοστατίνης (οκτρεοτίδη, λανρεοτίδη) και οι νεότερες μορφές τους μακράς διάρκειας (LAR) αποτελούν τη θεραπεία εκλογής για την αντιμετώπιση του καρκινοειδούς συνδρόμου των λειτουργικών ΝΕΝ. Η δράση τους ασκείται μέσω δέσμευσης με τους υποδοχείς σωματοστατίνης (SSTR), κυρίως τύπου 2 (SSTR2). Σημαντική εξέλιξη στην ιστορική διαδρομή των ΝΕΝ αποτέλεσε η τεκμηρίωση και της αντινεοπλασματικής δράσης των SSTA. Η αντινεοπλασματική τους ιδιότητα μπορεί να είναι αποτέλεσμα είτε άμεσης δράσης με την μεσολάβηση των SSTR που οδηγεί σε απόπτωση και αναστολή του κυτταρικού κύκλου είτε έμμεσης μέσω αναστολής της αγγειογένεσης και απελευθέρωσης τροφικών ή αυξητικών παραγόντων (15).
Η δέσμευση της οκτρεοτίδης στους SSTR επάγει την παραγωγή ειδικών πρωτεϊνών G.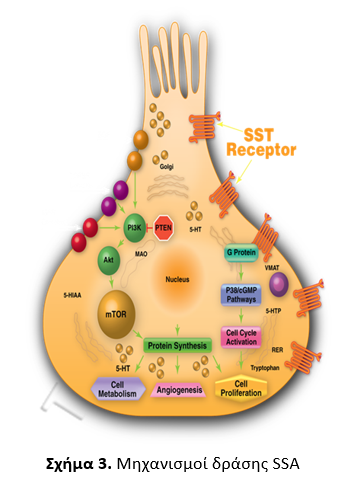
Οι πρωτείνες G ενεργοποιούν φωσφωτυροσινικές φωσφατάσες,
με επακόλουθη αναστολή της τυροσινικής κινάσης πρωτεϊνικών μορίων που συμμετέχουν σε κρίσιμες οδούς
μεταγωγής σημάτων.
Η αναστολή της MAPK, όπως και του βιόδρομου PI3K/Akt/mTOR,
μέσω των SSTR2, έχει συνδεθεί με την αντιπολλαπλασιαστική
δράση της οκτρεοτίδης (16
7. Τυχαιοποιημένες μελέτες καθιέρωσης εγκεκριμένων συστηματικών θεραπειών ΝΕΝ
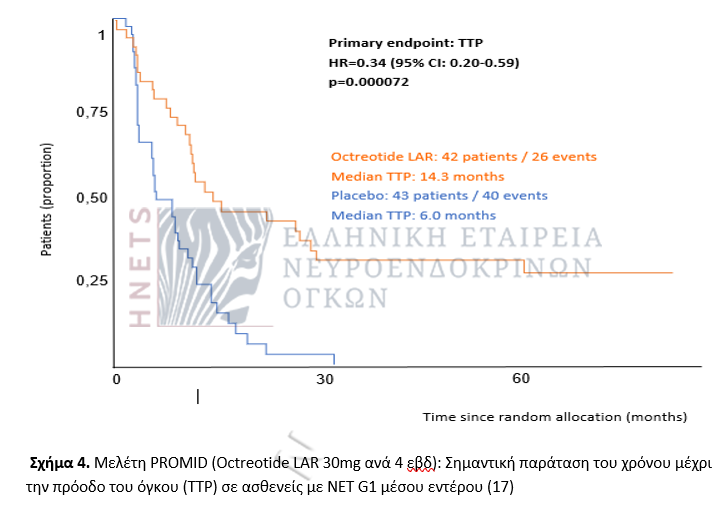
Μελέτη PROMID
Η PROMID είναι η πρώτη προοπτική μελέτη που κατέδειξε την αντινεοπλασματική δράση της οκτρεοτίδης σε νεοδιαγνωσμένους ασθενείς με προχωρημένα ανεγχείρητα ή μεταστατικά, λειτουργικά ή μη, καλά διαφοροποιημένα ΝΕΤ του μέσου εντέρου. Η οκτρεοτίδη ελάττωσε τον κίνδυνο προόδου της νόσου (ΤΤΡ) κατά 66% και ευνόησε ιδιαίτερα τους ασθενείς με φορτίο ηπατικής νόσου <10% .
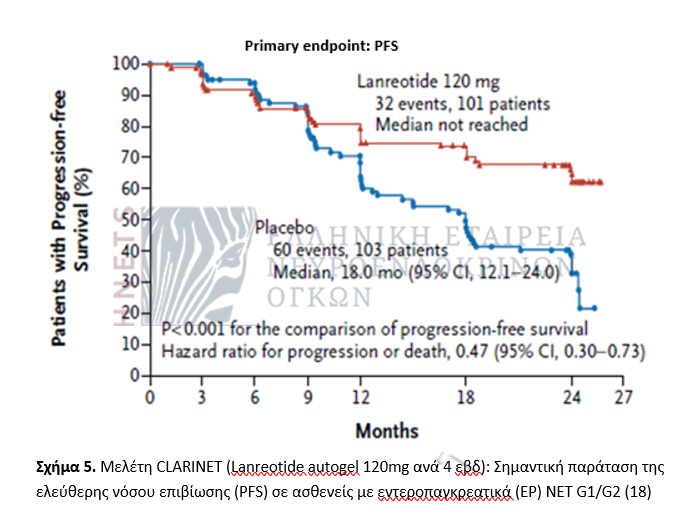
Μελέτη CLARINET
H Clarinet, επίσης τυχαιοποιημένη διπλή-τυφλή μελέτη, αξιολόγησε την λανρεοτίδη σε ασθενείς με προχωρημένα ανεγχείρητα ή μεταστατικά εντεροπαγκρεατικά (EP) ΝΕΤ, καλής ή μέτριας διαφοροποίησης (G1 ή G2) με Ki-67<10%, μη λειτουργικά, με θετικό Octreoscan και χωρίς πρόοδο πριν την τυχαιοποίησή τους. Η λανρεοτίδη παράτεινε σημαντικά την ελεύθερη προόδου επιβίωση (PFS) και το όφελος αφορούσε σε όλες τις υποομάδες ανεξάρτητα της προέλευσης του όγκου, του βαθμού διαφοροποίησής του και του μεταστατικού φορτίου του ήπατος. Τα ευρήματα αυτά, σε συνδυασμό με το ευνοϊκό προφίλ τοξικότητας, υποστηρίζουν την πρώιμη χρήση της στο θεραπευτικό αλγόριθμο ασθενών με EP-NEN (18).
Στοχευμένες θεραπείες
Μελέτη SUNITINIB
Η σουνιτινίμπη είναι αναστολέας τυροσινικής κινάσης (ΤΚΙ) που στοχεύει τη σηματοδότηση των οδών VEGFR και PDGFR και έχει δράση στα παγκρεατικά ΝΕΤ (Ρ-ΝΕΤ). Η σουνιτινίμπη δοκιμάσθηκε σε πολυεθνική διπλή-τυφλή τυχαιοποιημένη μελέτη με συνεχή χορήγηση 37,5mg ημερησίως σε ασθενείς με προχωρημένα καλά διαφοροποιημένα ΝΕΤ παγκρέατος και τεκμηριωμένη πρόοδο νόσου το τελευταίο 12μηνο. Συγκριτικά με τους ασθενείς της ομάδας εικονικού φαρμάκου, εκείνοι που έλαβαν σουνιτινίμπη πέτυχαν σημαντική βελτίωση του PFS που αποτελούσε τον κύριο καταληκτικό στόχο, της ανταπόκρισης και της συνολικής επιβίωσης.
H αγωγή ήταν καλά ανεκτή και οι συνηθέστερες παρενέργειες ήταν διάρροια, ναυτία, ασθένεια, εμετό και κόπωση, καθεμία σε συχνότητα περίπου 30% (19).
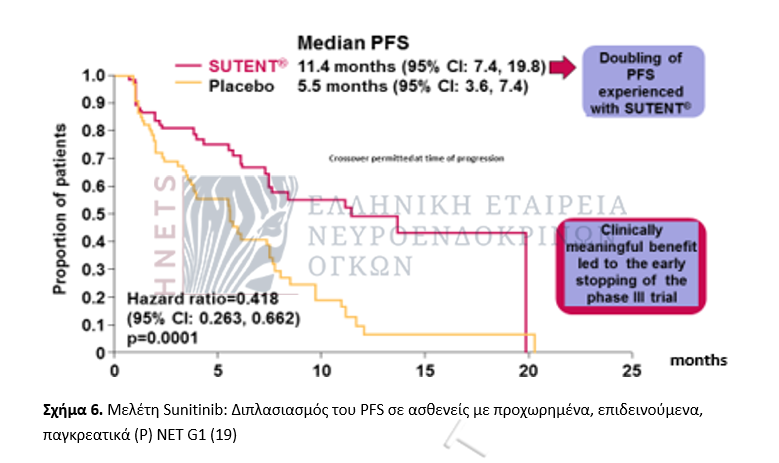
Μελέτη RADIANT-3
Η εβερολίμη, αναστολέας του mammalian target of rapamycin (mTOR) έχει επίσης δραστηριότητα στα Ρ-ΝΕΤ. Η RADIANT-3 είναι τυχαιοποιημένη φάσης 3 μελέτη με ημερήσια χορήγηση 10mg εβερολίμης ή εικονικού φαρμάκου σε ασθενείς με προχωρημένα Ρ-ΝΕΤ, καλής ή μέσης διαφοροποίηση και απεικονιστική επιδείνωση εντός των τελευταίων 12 μηνών.
Η εβερολίμη παράτεινε σημαντικά το PFS και μείωσε κατά 66% τον κίνδυνο προόδου της νόσου ή θανάτου. Οι ανεπιθύμητες παρενέργειες, κυρίως grade 1-2, συνηθέστερα ήταν στοματίτιδα, εξάνθημα, διάρροια, κόπωση και λοιμώξεις πρωτίστως αναπνευστικές (20).
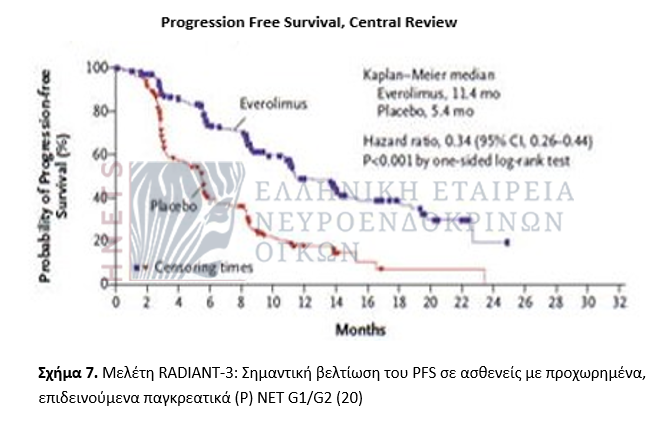
Μελέτη RADIANT-4
H RADIANT-4, τυχαιοποιημένη διπλή-τυφλή μελέτη φάσης 3, αξιολόγησε την εβερολίμη σε ασθενείς με προχωρημένα, επιδεινούμενα, μη λειτουργικά, καλά διαφοροποιημένα γαστρεντερικά ή πνευμονικά ΝΕΤ. Η εβερολίμη σε δόση 10mg/ημερησίως, συγκρινόμενη με το εικονικό φάρμακο, παράτεινε κατά 7,1 μήνες το διάμεσο PFS (11 vs 3,9 μήνες) και μείωσε κατά 52% τον κίνδυνο προόδου ή θανάτου (21).
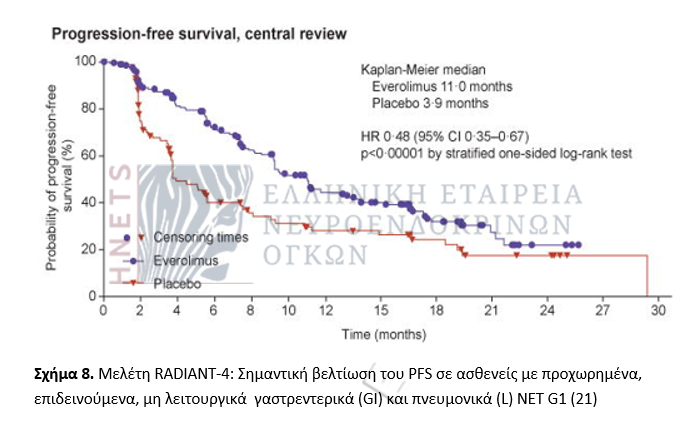
Peptide Receptor Radionuclide Therapy (PRRT)
Ασθενείς με προχωρημένα καλά διαφοροποιημένα ΝΕΤ μέσου εντέρου και πρόοδο νόσου υπό θεραπεία 1ης γραμμής με ανάλογα σωματοστοτίνης έχουν περιοριορισμένες θεραπευτικές δυνατότητες.
Η εφαρμογή Peptide Receptor Radionuclide Therapy (PRRT) αποτελεί στοχευμένη θεραπευτική επιλογή. H δομή της φαίνεται στο σχήμα 9.
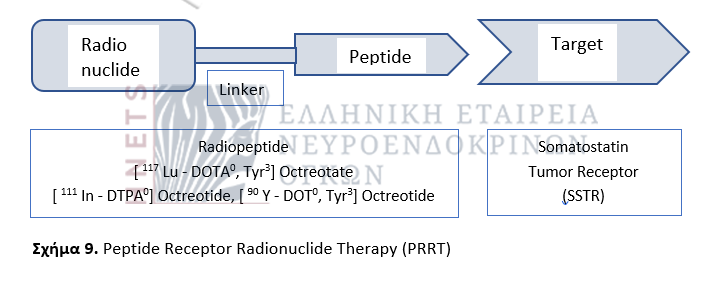
Μελέτη NETTER-1
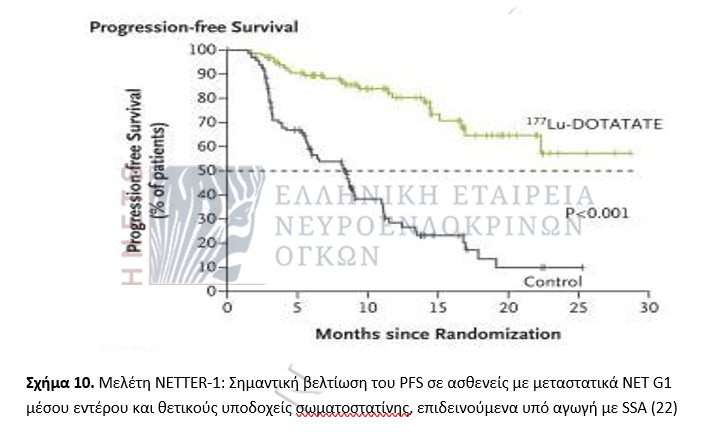
Στη μελέτη NETTER-1 εκτιμήθηκε η αποτελεσματικότητα και ασφάλεια της χορήγησης Lutetium-177 (177Lu)–Dotatate σε ασθενείς με μεταστατικά, επιδεινούμενα ΝΕΤ G1 μέσου εντέρου και θετικούς υποδοχείς σωματοστατίνης. Οι ασθενείς τυχαιοποιήθηκαν στη λήψη είτε 177Lu-Dotatate (4 εγχύσεις των 7,4GBq ανά 8 εβδομάδες) μαζί με Octreotide LAR 30 mg ανά 4 εβδομάδες είτε Octreotide LAR στη διπλάσια δόση των 60 mg ανά 4 εβδομάδες. Η θεραπεία με PRRT, συγκρινόμενη με την υψηλή δοσολογία Octreotide, απέδωσε σημαντική επιμήκυνση του PFS, του κύριου καταληκτικού σημείου της μελέτης, και σημαντικά καλύτερες ανταποκρίσεις. Κλινικά σημαντική μυελοτοξικότητα παρατηρήθηκε σε ποσοστό ασθενών μικρότερο του 10% (22).
8. Αντιμετώπιση καρκινοειδούς συνδρόμου
- Τα ανάλογα σωματοστατίνης (SSA) αποτελούν την πρώτη επιλογή για την αντιμετώπιση των συμπτωμάτων του καρκινικού συνδρόμου και των καρδιακών διαταραχών που σχετίζονται με τα λειτουργικά ΝΕΝ.
- Η IFN-α μπορεί να βοηθήσει ως θεραπεία 2ης γραμμής αλλά η χρήση της έχει υποχωρήσει λόγω του τοξικού της προφίλ.
- Σημαντική εξέλιξη στην αντιμετώπιση του καρκινοειδούς συνδρόμου και ειδικότερα της διάρροιας που είναι ανθεκτική στην χορήγηση ανάλογων σωματοστατίνης, αποτελεί η χρήση του telotristat etitrate, αναστολέα της παραγωγής σεροτονίνης (σχήμα 10).
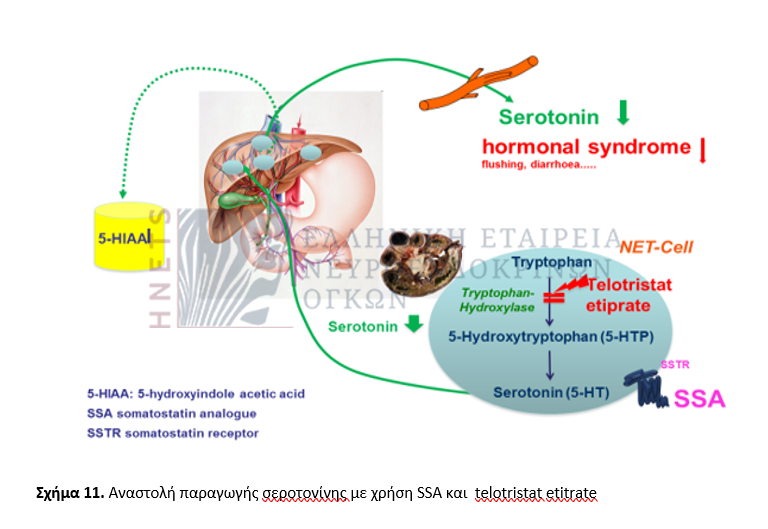
Η μελέτη ΤΕLESTAR, διπλή-τυφλή φάσης 3, αξιολόγησε την αποτελεσματικότητα του telotristat ethyl στη μείωση του αριθμού των ημερήσιων κενώσεων σε ασθενείς με ανθεκτική διάρροια υπό θεραπεία με SSA. Σε ασθενείς με ανεπαρκή έλεγχο του καρκινοειδούς συνδρόμου υπό SSA, η προσθήκη telotristat ethyl βελτίωσε σημαντικά τις διαρροϊκές κενώσεις και ήταν καλά ανεκτό. Η ελάττωση των επιπέδων 5-HIAA στα ούρα 24ώρου ήταν επίσης σημαντική, ενώ υπήρχε και βελτίωση αλλά όχι στατιστικά σημαντική των εξάψεων (23)
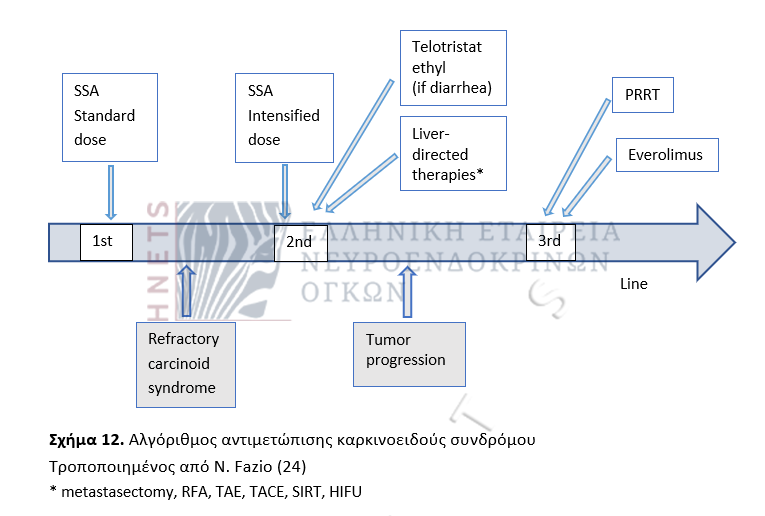
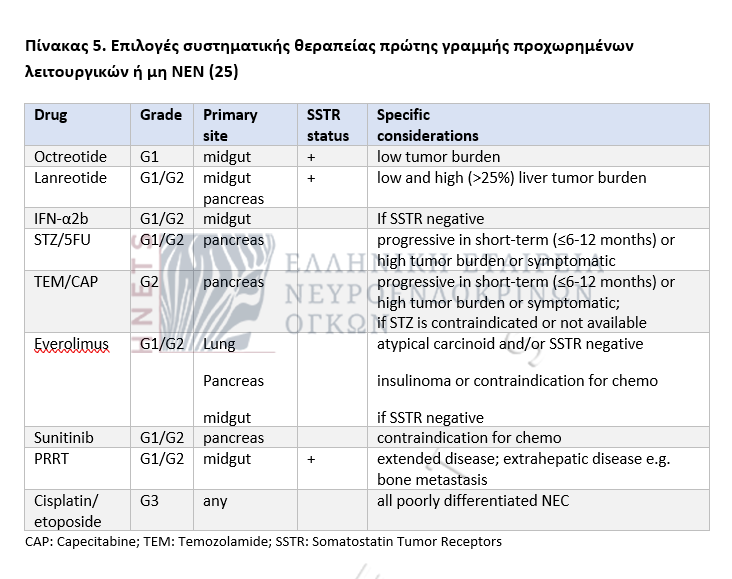
9. Θεραπευτικοί αλγόριθμοι προχωρημένων εντεροπαγκρεατικών ΝΕΝ - Συστηματική θεραπεία πρώτης γραμμής προχωρημένων ΝΕΝ - Θεραπευτικές επιλογές NEC/NETG3
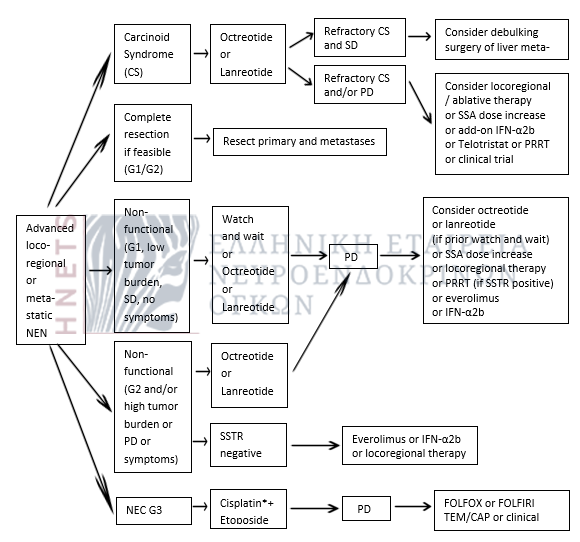
Σχήμα 13. Θεραπευτικός αλγόριθμος τοπικά προχωρημένων ή/και μεταστατικών εντερικών (midgut) ΝΕΝ (25)
PD: progressive disease; SD: stable disease; TEM/CAP: temozolomide/capecitabine;
* Cisplatin may be replaced by carboplatin
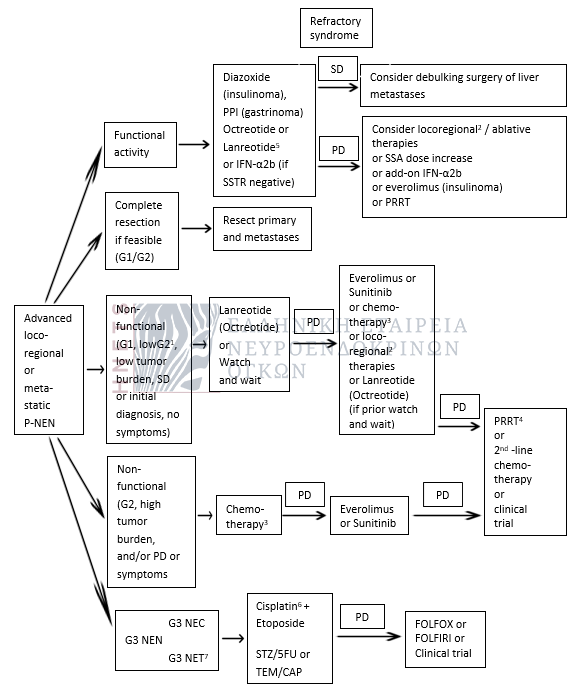
Σχήμα 14. Θεραπευτικός αλγόριθμος τοπικά προχωρημένων ή/και μεταστατικών παγκρεατικών ΝΕΝ (P-NEN) (25)
1 Ki-67 <5-10%; 2 locoregional therapies are contraindicated after Whipple procedure; 3 recommended regimens include STZ/5FU or doxorubicin, TEM/CAP is an alternative scheme if STZ is contraindicated or not available; 4 if SSTR imaging is positive; 5 patients should be monitored for paradoxical reaction (increasing hypoglycemia); 6 cisplatin may be replaced by carboplatin; 7G3 NET is coined for tumors with Ki-67 >20% but well or moderately differentiated morphology; SD: stable disease; PD: progressive disease; TEM/CAP: temozolomide/capecitabine
The term “or” indicates that the use of the other options at further progression should be considered.

10. Παρατηρήσεις και επισημάνσεις στη διαχείρηση ΝΕΝ
- Τα ΝΕΝ χαρακτηρίζονται από μεγάλη ετερογένεια και ποικίλη βιολογική συμπεριφορά εξαρτώμενη από την εστία προέλευσής τους.
- Ο βαθμός κακοήθειας (grade) αποτελεί σημαντικό παράγοντα καθοδήγησης της θεραπείας και για παράδειγμα η χημειοθεραπεία είναι η αγωγή 1ης γραμμής σε NEΝ G3.
- Τα ανάλογα σωματοστατίνης (SSA) αποτελούν τη θεραπεία 1ης γραμμής, μακράς συνήθως διάρκειας, σε ασθενείς με λειτουργικά ΝΕΝ και καρκινοειδές σύνδρομο.
- SSA συνιστώνται και σε ασθενείς με προχωρημένα, αργά αναπτυσσόμενα, μη λειτουργικά, καλά διαφοροποιημένα γαστρεντεροπαγκρεατικά (GEP) NEN. Η σύσταση κατ΄ επέκταση αφορά και τα αντίστοιχα πνευμονικά ΝΕΝ.
- Η ανταπόκριση στα SSA είναι συνήθως σταθεροποίηση της νόσου.
- SSA δεν συνιστώνται σε NEC G3.
- Επίσης δεν συνιστάται η χρήση SSA για επικουρική θεραπεία.
- Η συνέχιση SSA επί προόδου προχωρημένων, μη λειτουργικών ΝΕΤ αποτελούσε ζήτημα αμφισβήτησης. Πρόσφατα δεδομένα υποστηρίζουν τη δυνατότητα εντατικοποίησης της δοσολογίας SSA πριν την απόφαση αλλαγής σε άλλη γραμμή θεραπείας ενδεχομένως τοξικότερης. Η μελέτη CLARINET FORTE, προοπτική ανοιχτή ευρωπαϊκή μελέτη φάσης 2, εξετάζει την αποτελεσματικότητα και ασφάλεια πύκνωσης της συχνότητας χορήγησης Lanreotide autogel 120mg ανά 14 ημέρες, αντί της συνήθους ανά 28 ημέρες, σε ασθενείς με επιδεινούμενα ΝΕΤ παγκρέατος (με Ki67 ≤10%) ή μέσου εντέρου. Η συχνότερη ανά 14 ημέρες λήψη Lanreotide autogel 120mg ήταν ασφαλής και απέδωσε ελπιδοφόρα αποτελέσματα αναφορικά με τα ποσοστά ελέγχου της νόσου και το PFS (8,3 μήνες για τα ΝΕΤ μέσου εντέρου και 5,6 μήνες για τα ΝΕΤ παγκρέατος) (26) .
- Για τις θεραπευτικές αποφάσεις, πέραν της εντόπισης της πρωτοπαθούς όγκου και του grade, πρέπει να ληφθούν υπόψη το φορτίο όγκου και ο ρυθμός εξέλιξής του:
- Για παγκρεατικά NET G1/G2 μπορούμε να χορηγήσουμε αρχικά SSA και εφόσον υπάρχει αργή εξέλιξη να προχωρήσουμε σε στοχευτικούς παράγοντες, sunitinib ή everolimus.
- Για παγκρεατικά NET με μεγάλο φορτίο όγκου ή ταχεία εξέλιξη είναι προτιμότερη η χορήγηση χημειοθεραπείας με σχήματα STZ/5FU ή TEM/CAP. Χημειοθεραπεία μπορεί επίσης να χορηγηθεί μετά τους στοχευτικούς παράγοντες επί εξέλιξης της νόσου έστω και αργής. Στις περιπτώσεις αυτές η εφαρμογή PRRT (Lutetium-177 DOTATE) εξετάζεται ως θεραπεία 3ης ή 4ης γραμμής.
- Για ΝΕΤ G1/G2 μέσου εντέρου, λειτουργικά ή μη, ενδείκνυται έναρξη θεραπείας με SSA. Επί προόδου το sunitinib δεν έχει θέση αλλά με βάση τη μελέτη RADIANT 4 μπορεί να χορηγηθεί το everolimus. Χρήση PRRT (Lutetium-177 DOTATE) μπορεί να αποτελεί θεραπεία 2ης γραμμής με βάση τη μελέτη NETTER-1. - Κατά τη διαδρομή της νόσου και με την πάροδο του χρόνου οι ασθενείς οδεύουν συχνά από μια θεραπευτική μέθοδο σε άλλη με την κατάλληλη υποστήριξη εξειδικευμένων ιατρών. Οι ιδιαιτερότητες των ασθενών με ΝΕΝ επιβάλλουν την παραπομπή τους σε ειδικά κέντρα. Η αντιμετώπιση σε τέτοια έμπειρα κέντρα βελτιώνει σημαντικά την επιβίωση των ασθενών με ΝΕΝ (8, 27).
11. Εξελίξεις και προοπτικές
- Συνδυασμοί SSA και temozolomide αποτελούν ήδη αντικείμενο κλινικών έρευνας.
- Η Γερμανική φάσης 2 μελέτη SONNET δοκιμάζει το συνδυασμό lanreotide - temozolomide σε προχωρημένα, προθεραπευμένα, επιδεινούμενα ΝΕΤ G1/G2 γαστρεντεροπαγκρεατικά ή άγνωστης προέλευσης. Προκαταρκτικά αποτελέσματα δείχνουν ευνοϊκό ποσοστό ελέγχου της νόσου στους 6 μήνες σε 73,5% των ασθενών και διάμεσο PFS 11,1 μηνών (28) .
- Στην Ιταλική προοπτική μελέτη ATLANT ο ίδιος συνδυασμός σε ασθενείς με προχωρημένα, προθεραπευμένα, επιδεινούμενα θωρακικά ΝΕΤ πνεύμονα και θύμου, έδειξε επίσης ελπιδοφόρα ποσοστά ελέγχου της νόσου (29
- Η δράση νέων αντιαγγειογενετικών παραγόντων, όπως το surufatinib, έχει δοκιμαστεί σε δύο κινεζικές μελέτες φάσης 3 (SANET-p και SANET-ep) σε ασθενείς με προχωρημένα, καλά διαφοροποιημένα NET είτε παγκρεατικά (30) ή εξωπαγκρεατικά (31). Σε αμφότερες τις μελέτες διαπιστώθηκε σημαντική βελτίωση του PFS ώστε το surufatinib να αποτελεί θεραπευτική επιλογή στους ασθενείς αυτούς.
- Τα ΝΕΝ αποτελούν πεδίο συνεχών αναζητήσεων και εντατικής βασικής και κλινικής έρευνας. Οι ερευνητικές προσπάθειες στοχεύουν:
- Τη διευκρίνιση των υποκείμενων μοριακών μηχανισμών.
- Την αναγνώριση του ανοσολογικού τοπίου και του μικροπεριβάλλοντος του όγκου.
- Τη χρήση νέων απεικονιστικών κριτηρίων για ασφαλέστερη αξιολόγηση της θεραπευτικής απάντησης.
- Την αποκάλυψη προβλεπτικών βιοδεικτών, όπως NETest, CTCs, cDNA/cRNA.
- Οι νευροενδοκρινείς όγκοι έχουν μικρό φορτίο μεταλλάξεων που δικαιολογεί τον χαρακτηρισμό της ανοσολογικής ερήμου. Η δραστηριότητα των αναστολέων των σημείων ελέγχου (check point inhibitors) στα ΝΕΤ G1/G2 είναι γενικά περιορισμένη ή και απούσα. Σε μελέτη φάσης 2 τo spartalizumab, αναστολέας PD-1, χορηγήθηκε σε προχωρημένα μη λειτουργικά ΝΕΝ με Ki-67≥10% (NET G2/G3 και NEC). Διαπιστώθηκε ότι αυξημένη συγκέντρωση των ανοσοκυττάρων Τ-Reg (ΤΙΜ3+) προδίκαζε έλλειψη απάντησης σε ασθενείς με GEP-NEC. Αντίθετα αυξημένη διήθηση με κύτταρα CD8+ ευνοούσε ανταποκρίσεις σε ασθενείς με ΝΕΤ G2/G3 και NEC (32). Περαιτέρω μελέτες με PD-L1 αναστολείς, όπως nivolumab και pembrolizumab, βρίσκονται σε εξέλιξη. Ιδιαίτερα ενδιαφέρουσες είναι οι έρευνες μετατροπής των ΝΕΝ σε “φλεγμονώδεις” όγκους και η επαγωγή ανοσογονικότητας με ογκολυτικούς ιούς και ανοσοτροποποιητικούς παράγοντες όπως οι αγωνιστές των Toll-like υποδοχέων. Η εφαρμογή PRRT και οι τοπικοπεριοχικοί χειρισμοί των ηπατικών μεταστάσεων με RFA, TAE, SIRT μπορούν να πυροδοτήσουν φλεγμονώδη απάντηση. Σε κλινική δοκιμή φάσης I μελετάται το διειδικό αντίσωμα XmAb18087 που στοχεύει τον υποδοχέα SSTR2 και τα D3 κύτταρα σε ασθενείς με καλά διαφοροποιημένα ΝΕΝ. Ενδιαφέρουσα είναι επίσης η απεικονιστική παρακολούθηση της άνοσης απάντησης με IFN-γ PET.
- Συνδυασμοί SSA και temozolomide αποτελούν ήδη αντικείμενο κλινικών έρευνας. - Η Γερμανική φάσης 2 μελέτη SONNET δοκιμάζει το συνδυασμό lanreotide - temozolomide σε προχωρημένα, προθεραπευμένα, επιδεινούμενα ΝΕΤ G1/G2 γαστρεντεροπαγκρεατικά ή άγνωστης προέλευσης. Προκαταρκτικά αποτελέσματα δείχνουν ευνοϊκό ποσοστό ελέγχου της νόσου στους 6 μήνες σε 73,5% των ασθενών και διάμεσο PFS 11,1 μηνών (28) .
- - Στην Ιταλική προοπτική μελέτη ATLANT ο ίδιος συνδυασμός σε ασθενείς με προχωρημένα, προθεραπευμένα, επιδεινούμενα θωρακικά ΝΕΤ πνεύμονα και θύμου, έδειξε επίσης ελπιδοφόρα ποσοστά ελέγχου της νόσου (29).
- Η δράση νέων αντιαγγειογενετικών παραγόντων, όπως το surufatinib, έχει δοκιμαστεί σε δύο κινεζικές μελέτες φάσης 3 (SANET-p και SANET-ep) σε ασθενείς με προχωρημένα, καλά διαφοροποιημένα NET είτε παγκρεατικά (30) ή εξωπαγκρεατικά (31). Σε αμφότερες τις μελέτες διαπιστώθηκε σημαντική βελτίωση του PFS ώστε το surufatinib να αποτελεί θεραπευτική επιλογή στους ασθενείς αυτούς.
- Τα ΝΕΝ αποτελούν πεδίο συνεχών αναζητήσεων και εντατικής βασικής και κλινικής έρευνας. Οι ερευνητικές προσπάθειες στοχεύουν:
- Τη διευκρίνιση των υποκείμενων μοριακών μηχανισμών.
- Την αναγνώριση του ανοσολογικού τοπίου και του μικροπεριβάλλοντος του όγκου.
- Τη χρήση νέων απεικονιστικών κριτηρίων για ασφαλέστερη αξιολόγηση της θεραπευτικής απάντησης.
- Την αποκάλυψη προβλεπτικών βιοδεικτών, όπως NETest, CTCs, cDNA/cRNA. - Οι νευροενδοκρινείς όγκοι έχουν μικρό φορτίο μεταλλάξεων που δικαιολογεί τον χαρακτηρισμό της ανοσολογικής ερήμου. Η δραστηριότητα των αναστολέων των σημείων ελέγχου (check point inhibitors) στα ΝΕΤ G1/G2 είναι γενικά περιορισμένη ή και απούσα. Σε μελέτη φάσης 2 τo spartalizumab, αναστολέας PD-1, χορηγήθηκε σε προχωρημένα μη λειτουργικά ΝΕΝ με Ki-67≥10% (NET G2/G3 και NEC). Διαπιστώθηκε ότι αυξημένη συγκέντρωση των ανοσοκυττάρων Τ-Reg (ΤΙΜ3+) προδίκαζε έλλειψη απάντησης σε ασθενείς με GEP-NEC. Αντίθετα αυξημένη διήθηση με κύτταρα CD8+ ευνοούσε ανταποκρίσεις σε ασθενείς με ΝΕΤ G2/G3 και NEC (32). Περαιτέρω μελέτες με PD-L1 αναστολείς, όπως nivolumab και pembrolizumab, βρίσκονται σε εξέλιξη. Ιδιαίτερα ενδιαφέρουσες είναι οι έρευνες μετατροπής των ΝΕΝ σε “φλεγμονώδεις” όγκους και η επαγωγή ανοσογονικότητας με ογκολυτικούς ιούς και ανοσοτροποποιητικούς παράγοντες όπως οι αγωνιστές των Toll-like υποδοχέων. Η εφαρμογή PRRT και οι τοπικοπεριοχικοί χειρισμοί των ηπατικών μεταστάσεων με RFA, TAE, SIRT μπορούν να πυροδοτήσουν φλεγμονώδη απάντηση. Σε κλινική δοκιμή φάσης I μελετάται το διειδικό αντίσωμα XmAb18087 που στοχεύει τον υποδοχέα SSTR2 και τα D3 κύτταρα σε ασθενείς με καλά διαφοροποιημένα ΝΕΝ. Ενδιαφέρουσα είναι επίσης η απεικονιστική παρακολούθηση της άνοσης απάντησης με IFN-γ PET.
Βιβλιογραφία
1. Caplin ME, Buscombe JR, Hilson AJ, Jones AL, Watkinson AF, Burroughs AK. Carcinoid tumour. Lancet 1998, 352(9130):799-805.
2. Clark OH, Benson AB, Berlin JD, Choti MA, Doherty GM, Engstrom PF, Gibbs JF, Heslin MJ, Kessinger A, KulkeMH, Kvols L, Salem R, Saltz L, Shah MH, Shibata S, Strosberg JR, Yao JC. NCCN Neuroendocrine Tumors Panel Members. NCCN Clinical Practice Guidelines in Oncology: Neuroendocrine Tumors. J Natl Compr Cancer Netw 2009, 7(7):712-47.
3. Modlin IM, Kidd M, Latich I, N Zikusoka MN, D Shapiro MD. Current status of gastrointestinal carcinoids. Gastroenterology 2005, 128(6):1717-51.
4. National Comprehensive Cancer Network. NCCN Practice Guidelines in Oncology: Neuroendocrine Tumors, 2008.
5. Klöppel G, Perren A, Heitz PU. The gastroenteropancreatic neuroendocrine cell system and its tumors: the WHO classification. Ann NY Acad Sci 2004, 1014:13-27.
6. Strosberg JR, Nasir A, Hodul P, Kvols L. Biology and treatment of metastatic gastrointestinal neuroendocrine tumors. Gastrointest Cancer Res 2008, 2(3):113-25.
7. Berge T, Linell F. Carcinoid tumours. Frequency in a defined population during a 12-year period. Acta Pathol Microbiol Scand A 1976, 84(4):322-30.
8. Yao JC, Hassan M, Phan A, et al. One hundred years after “carcinoid”: Epidemiology of the prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol 2008, 26:3063-72.
9. Hauso O , Gustafsson BI, Kidd M, Waldum HL, Drozdov I, Chan AKC, Modlin IM. Neuroendocrine tumor epidemiology: contrasting Norway and North America. Cancer 2008, 113(10):2655-64.
10. Modlin IM , Champaneria MC, Chan AKC, Kidd M. A three-decade analysis of 3,911 small intestinal neuroendocrine tumors: the rapid pace of no progress. Am J Gastroenterol 2007, 102(7):1464-73.
11. Soga J. Early-stage carcinoids of the gastrointestinal tract: an analysis of 1914 reported cases. Cancer 2005, 103(8):1587-95.
12. Ramage JK, Ahmed A, Ardill J, Bax N, Breen DJ, Caplin ME, Corrie P, Davar J, Davies AH, Lewington V, Meyer T, Newell-Price J, Poston G, Reed N, Rockall A, Steward W, Thakker RV, Toubanakis C, Valle J, Verbeke C, Grossman AB, UK and Ireland Neuroendocrine Tumour Society. Guidelines for the management of gastroenteropancreatic neuroendocrine (including carcinoid) tumours (NETs). Gut 2012, 61(1):6-32.
13. Caplin M. Overview of management of NETS, 7th ENETS Postgraduate Course 2017.
14. Garcia-Carbonero R, H. Sorbye H, Baudin E, Raymond E, Wiedenmann B, Niederle B, Sedlackova E, Toumpanakis C, Anlauf M, Cwikla JB, Caplin M, O’Toole D, Perren A. ENETS Consensus Guidelines for High-Grade Gastroenteropancreatic Neuroendocrine Tumors and Neuroendocrine Carcinomas. Neuroendocrinology 2016, 103:186-94.
15. Susini C, Buscail L: Rationale for the use of somatostatin analogs as antitumor agents. Ann Oncol 2006,17: 1733-42.
16. Florio T: Molecular mechanisms of the antiproliferative activity of somatostatin receptors (SSTRs) in neuroendocrine tumors. Front Biosci 2008, 13: 822-40.
17. Rinke A, Müller H-H, Schade-Brittinger C, Klose K-J, Barth P, Wied M, Mayer C, Aminossadati B, Pape U-F, Bläker M, Harder J, Arnold C, Gress T, Arnold R, PROMID Study Group. Placebo-controlled, double-blind, prospective, randomized study on the effect of octreotide LAR in the control of tumor growth in patients with metastatic neuroendocrine midgut tumors: a report from the PROMID Study Group. J Clin Oncol. 2009;27(28):4656-63.
18. Caplin ΜΕ, Pavel Μ, Ćwikła JB, Phan AT, Raderer M, Sedláčková E, Cadiot G, Wolin EM, Capdevila J, Wall L, Rindi G, Langle A, Martinez S, Blumberg J, Ruszniewski P, CLARINET Investigators. Lanreotide in metastatic enteropancreatic neuroendocrine tumors. N Engl J Med 2014, 371(3):224-33.
19. Raymond Ε, Dahan L, Raoul J-L, Bang Y-J, Borbath I, Lombard-Bohas C, Valle J, Metrakos P, Smith D, Vinik A, Chen J-S, Hörsch D, Hammel P, Wiedenmann B, Cutsem EV, Patyna S, Lu DR, Blanckmeister C, Chao R, Ruszniewski P. Sunitinib malate for the treatment of pancreatic neuroendocrine tumors. N Engl J M 2011, 364(6):501-13.
20. Yao JC, Shah MH, Ito T, Bohas CL, Wolin EM, Cutsem EV, Hobday TJ, Okusaka T, Capdevila J, de Vries EGE, Tomassetti P, Pavel ME, Hoosen S, Haas T, Lincy J, Lebwohl D, Öberg K, RAD001 in Advanced Neuroendocrine Tumors, Third Trial (RADIANT-3) Study Group. Everolimus for advanced pancreatic neuroendocrine tumors. N Engl J M 2011, 364(6):514-23.
21. Yao JC, Fazio N, Singh S, Buzzoni R, Carnaghi C, Wolin E, Tomasek J, Raderer M, Lahner H, Voi M, Pacaud LB, Rouyrre N, Sachs C, Valle JW, Fave GD, Cutsem EV, Tesselaar M, Shimada Y, Oh D-Y, Strosberg J, Kulke MH, Pavel ME, RAD001 in Advanced Neuroendocrine Tumours, Fourth Trial (RADIANT-4) Study Group. Everolimus for the treatment of advanced, non-functional neuroendocrine tumours of the lung or gastrointestinal tract (RADIANT-4): a randomised, placebo-controlled, phase 3 study. Lancet 2016, 387(10022):968-77.
22. Strosberg J, El-Haddad G, Wolin E, Hendifar A, Yao J, Chasen B, Mittra E, Kunz PL, Kulke MH, Jacene H, Bushnell D, O'Dorisio TM, Baum RP, Kulkarni HR, Caplin M, Lebtahi R, Hobday T, Delpassand E, Cutsem EV, Benson A, Srirajaskanthan R, Pavel M, Mora J, Berlin J, Grande E, Reed N, Seregni E, Öberg K, Sierra ML, Santoro P, Thevenet T, Erion JL, Ruszniewski P, Kwekkeboom D, Krenning E, NETTER-1 Trial Investigators. Phase 3 Trial of 177 Lu-Dotatate for Midgut Neuroendocrine Tumors. N Engl J M 2017, 376(2):125-35.
23. Pavel M, Gross DJ, Benavent M, Perros P, Srirajaskanthan R, Warner RRP, Kulke MH, Anthony LB, Kunz PL, Hörsch H, Weickert MO, Lapuerta P, Jiang W, Kassler-Taub K, Wason S, Fleming R, Fleming D, Garcia-Carbonero R. Telotristat ethyl in carcinoid syndrome: safety and efficacy in the TELECAST phase 3 trial. Endocr Relat Cancer 2018, 25(3):309-22.
24. Fazio N. Somatostatin Analogs. 2019-ESMO-Preceptorship-GEP-NET.
25. Pavel M, O’Toole D, Costa F, Capdevila J, Gross D, Kianmanesh R, Krenning E, Knigge U, Salazar R, Pape UF, Öberg K. ENETS Consensus Guidelines Update for the Management of Distant Metastatic Disease of Intestinal, Pancreatic, Bronchial Neuroendocrine Neoplasms (NEN) and NEN of Unknown Primary Site. Neuroendocrinology 2016, 103:172-85.
26. Pavel Μ, Ćwikła JB , Lombard-Bohas C , Borbath I , Shah T , Pape U-F, Truong Thanh X-M, Houchard A , Ruszniewski P. Efficacy and safety of lanreotide auto gel 120 mg every 14 days in progressive pancreatic or midgut neuroendocrine tumours: CLARINET FORTE study results. ESMO Virtual 2020, 1162MO.
27. Strosberg J, Gardner N, Kvols L. Survival and prognostic factor analysis of 146 metastatic neuroendocrine tumors of the mid-gut. Neuroendocrinology 2009, 89(4):471-76.
28. Pavel M, Denecke T, Lahner H, Horsch D, Rinke A, Koch A, Liyanage N, Raspel A, Pape UF, Raderer M. Disease control in progressive pancreatic and intestinal neuroendocrine tumors by combined treatment with lanreotide autogel and temozolomide: The SONNET study. 15th Annual ENETS Conference 2018, Abstr≠H19.
29. Ferolla P, Berruti A, Spada F, Brizzi MP, Ibrahim T, Colao A, Faggiano A, Marconcini R, Vaccaro V, Giuffrida D, Ghizzoni S, Houchard A, Fazio N. Lanreotide autogel (LAN) and temozolomide (TMZ) combination therapy in progressive thoracic neuroendocrine tumours (TNETs): ATLANT study results. ESMO Virtual Congress 2020. Abstr≠1161MO. Ann Oncol 2020, 31 (suppl 4): S711-S724.
30. Xu J, Shen L, Bai C, Wang W, Li J, Yu X, Li Z, Li E, Yuan X, Chi Y, Yin Y, Lou W, Xu N, Bai Y, Zhang T, Xiu D, Wang X, Yuan Y, Chen J, Qin S, Jia R, Lu M, Cheng Y, Zhou Z, Li J, He J, Su W. Surufatinib in advanced pancreatic neuroendocrine tumours (SANET-p): a randomised, double-blind, placebo-controlled, phase 3 study. Lancet Oncol 2020, 21(11):1489-99.
31. Xu J, Shen L, Zhou Z, Li J, Bai C, Chi Y, Li Z, Xu N, Li E, Liu T, Bai Y, Yuan Y, Li X, Wang X, Chen J, Ying J, Yu X, Qin S, Yuan X, Zhang T, Deng Y, Xiu D, Cheng Y, Tao M, Jia R, Wang W, Li J, Fan S, Peng M, Su W. Surufatinib in advanced extrapancreatic neuroendocrine tumours (SANET-ep): a randomised, double-blind, placebo-controlled, phase 3 study. Lancet Oncol 2020, 21(11):1500-12.
32. Yao JC, Strosberg J, Fazio N, Pavel ME, Ruszniewski P, Bergsland E, Li D, Tafuto S, Raj N, Campana D, Hijioka S, Raderer M, Guimbaud R, Gajate P, Pusceddu S, Reising A, Degtyarev E, Mookerjee B, Aimone P, Singh S. Activity & safety of spartalizumab (PDR001) in patients (pts) with advanced neuroendocrine tumors (NET) of pancreatic (Pan), gastrointestinal (GI), or thoracic (T) origin, & gastroenteropancreatic neuroendocrine carcinoma (GEP NEC) who have progressed on prior treatment (Tx). ESMO Congress 2018. Abstr≠3442. Ann Oncol 2018, 29 (suppl 8): viii467-viii478.



